
Anécdotas de la ciencia
Pese a que hay transcurrido ya cincuenta años, recuerdo todavía las clases de mi profesor de química en COU, el cual nos la enseñaba -y sabía mucha- desde un enfoque histórico y, si se me apura, anecdótico, lo que me permitió aprenderla de una manera amena e influyó de manera decisiva en mi elección posterior de estudiar esta disciplina en la universidad. Aquí intento recoger su testigo, dedicando este artículo a lo que he denominado anécdotas científicas aunque muchas de ellas si no todas de anecdóticas tienen poco. Lo que sí pretendo es contar episodios interesantes o curiosos de forma que estén al alcance de todos y les diviertan, o cuanto menos llamen su atención lo suficiente como para llegar hasta el final.
Dada su naturaleza rehúyo las explicaciones prolijas o aptas tan sólo para entendidos, así como de citas bibliográficas o reseñas que considero innecesarias dado que mi principal fuente de información ha sido internet y quien quiera profundizar en alguno de estos temas no tiene más que introducir su nombre en el buscador para encontrar toda la información que desee. Huelga decir que éste no es un trabajo de investigación ni pretende serlo y ni tan siquiera es original, ya que me he limitado a buscar y a extractar las historias que me interesaban, muchas de ellas oídas por vez primera a mi profesor.
El Premio Nobel de Albert Einstein
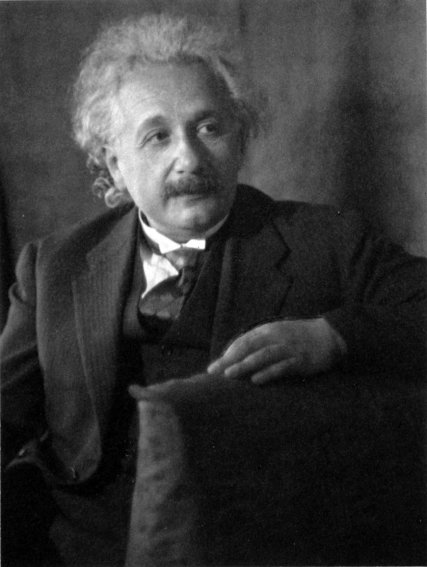
Albert Einstein
No existe la menor duda de que la principal aportación de Albert Einstein al acervo científico fue la Teoría de la Relatividad o mejor dicho las teorías, puesto que en realidad fueron dos: la Teoría de la Relatividad Especial, publicada en 1905, y la Teoría de la Relatividad General, que lo fue en 1915.
Asimismo recibió el Premio Nobel de Física en 1921, cuando ya era un renombrado científico. Si preguntamos a alguien por qué se lo concedieron, lo más probable es que responda que por la Teoría de la Relatividad, con lo cual se equivocará ya que en realidad lo fue por otro de sus descubrimientos, el efecto fotoeléctrico, que describió en 1905.
Aunque el efecto fotoeléctrico tiene unas aplicaciones prácticas de lo más cotidiano -por ejemplo en las puertas automáticas de los ascensores o de muchos establecimientos- mientras la Relatividad permanece en el plano de la física teórica, lo cierto es que no hace falta ser muy ducho en la materia para concluir que se trató de un premio de consolación, ya que esta última resultó ser uno de los pilares de la física moderna.
Así pues, la pregunta que surge de inmediato es: ¿por qué razón no se le concedió el Nobel por la Teoría de la Relatividad, sin discusión su obra cumbre y la razón por la que ha pasado a la historia de la ciencia? Al parecer, el veto a la Relatividad se debió a celos profesionales o bien por inquina personal, tanto da, por parte de los miembros del Comité Nobel o, más probablemente, de los seleccionadores encargados de nominar a los candidatos, pesando también prejuicios por el hecho de que Einstein era judío, de ideas socialistas y pacifista en una época en la que empezaban a estar en auge las ideologías opuestas.
De hecho, Einstein contó con dos enconados rivales que hicieron cuanto les fue posible por desacreditar sus descubrimientos: Philipp Lenard, un físico húngaro nacionalizado alemán que ganó el Nobel de Física en 1905 por sus investigaciones sobre los rayos catódicos, y Johannes Stark, físico alemán galardonado con este mismo premio en 1919 por el descubrimiento del efecto que lleva su nombre dentro de la espectroscopía.
Ambos, científicos renombrados, se convertirían años después en fervientes partidarios del nazismo, defendiendo una presunta ciencia aria en la que las teorías de Einstein estaban excluidas por su condición de judío. Aunque la polémica del Nobel que finalmente se le entregó a regañadientes fue anterior al surgimiento del nazismo, desde mucho antes tanto Lenard como Stark eran fervientes antisemitas, lo que probablemente influyó en el ostracismo al que éste y su teoría fueron sometidos.
¿Héroe o asesino?

Fritz Haber
Pese a que a diferencia de los controvertidos Premios Nobel de la Paz o de Literatura, los científicos deberían ser teóricamente más objetivos, el caso de Einstein no fue el único. Otro Nobel polémico fue el de Química de 1918, otorgado al químico alemán Fritz Haber por su descubrimiento de la síntesis del amoníaco, un compuesto fundamental en la industria química siendo una de sus aplicaciones la fabricación de abonos nitrogenados; también la de explosivos, pero ésta es otra historia.
Hasta entonces la única fuente natural de nitratos, la materia prima para estos fertilizantes, eran los enormes depósitos de guano -acumulaciones de excrementos de aves marinas- existentes en las islas o en territorios costeros del litoral pacífico sudamericano, principalmente los pertenecientes a Perú y Chile. Durante el siglo XIX fue un material estratégico del que los países desarrollados dependían de una manera similar a la que ocurre hoy en día con el petróleo, lo que llegó a provocar conflictos diplomáticos en incluso estuvo por medio de guerras como la del Pacífico entre España y la coalición de Chile y Perú entre 1865 y 1866, o la también llamada así que enfrentó a Chile con Perú y Bolivia entre 1879 y 1884.
El proceso de Haber, que es como se conoce a la síntesis del amoníaco a partir del nitrógeno atmosférico, acabó con el monopolio del guano al poderse obtener los abonos nitrogenados necesarios para la agricultura por procedimientos químicos sin dependencias externas, al tiempo que permitió incrementar notablemente el rendimiento agrícola. Así pues, excepto desde el punto de vista de los perjudicados exportadores de guano, no cabe la menor duda de que Haber se merecía sobradamente el galardón.
Pero... el mismo Haber que desarrolló la síntesis del amoníaco en 1911 fue el director del Departamento de Guerra Química del Ministerio de Guerra alemán durante la I Guerra Mundial, que utilizó gases tóxicos tales como el cloro, el fosgeno -dicloruro de carbonilo- o la terrible iperita o gas mostaza, un compuesto vesicante que en contacto con la piel, la córnea o las mucosas internas ocasiona úlceras de muy difícil curación. Y si bien por un lado salvó vidas alejando los riesgos de malas cosechas y hambrunas, por otro sembró la muerte y el horror en las trincheras.
Obviamente el Nobel le fue concedido por la síntesis del amoníaco y no por la guerra química, pero en 1918 las heridas de la I Guerra Mundial estaban todavía abiertas, por lo que era inevitable que la decisión del Comité Nobel resultase controvertida. Incluso la vida personal de Harber, que no renegó en ningún momento de su responsabilidad justificando la obligación de apoyar a su país en guerra, se vería afectada: su esposa, disconforme con sus actividades, se suicidó en 1915.
Años después, pese a su origen judío, los nazis le ofrecieron continuar sus investigaciones con armas químicas, a lo cual se negó exiliándose de Alemania y logrando que, paradójicamente, el régimen nazi acabara renegando de él y difamándolo al tiempo que aprovechaba sus descubrimientos anteriores para desarrollar venenos como el Zyklon B, de triste recuerdo por su uso en los campos de exterminio.
Harber falleció en Basilea en 1934, a los 65 años, de insuficiencia cardíaca. ¿Héroe? ¿Asesino? ¿O quizás tan sólo una víctima de las contradicciones de la difícil época en que le tocó vivir? Porque, ¿acaso fue menos asesino que quienes desarrollaron las bombas atómicas de Hiroshima y Nagasaki, o quienes lo hicieron con las bombas incendiarias que arrasaron Tokio o Dresde?
Una muerte absurda

Évariste Galois
Sin duda una de las muertes más innecesarias y absurdas de un científico fue la de Évariste Galois, un joven matemático francés nacido en 1811 y fallecido a los 20 años de edad víctima de un duelo.
Ya de adolescente había dado muestras sobradas de talento, aunque no destacó como escolar hasta que no empezó a estudiar matemáticas, momento en el que afloró su genio. Un genio lastrado por sus enfrentamientos académicos y políticos que se saldaron en expulsiones e incluso la cárcel, mientras escribía artículos matemáticos que fueron rechazados por las instituciones académicas pese a desarrollar en ellos soluciones a problemas que hoy se conocen como la teoría de Galois.
Seguía empeñado en intentar el reconocimiento de sus trabajos, difíciles de entender incluso por los matemáticos más prestigiosos de Francia, cuando recién salido de la cárcel se enredó en una pelea que acabó en desafío a un duelo. Cuenta la historia que la noche anterior, intuyendo su muerte, Galois se dedicó a escribir su testamento matemático describiendo apresuradamente su teoría, al que añadió los artículos que le habían sido rechazados.
Por desgracia para él y para la ciencia su premonición se cumplió, siendo herido de muerte y falleciendo al día siguiente con tan sólo veinte años de edad. Años después se publicaron al fin sus escritos, descubriéndose su valía y la gran aportación que supusieron para el avance de las matemáticas.
Pero él no pudo verlo y, todavía peor, tampoco pudo desarrollar su gran talento como hubiera ocurrido de no acaecer su prematura e innecesaria muerte.
El sueño de Kekulé
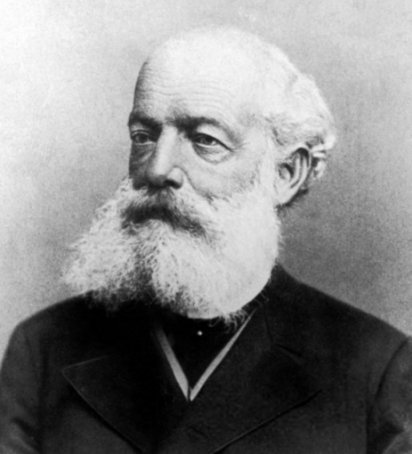
August Kekulé
Hora es que dejemos de hablar de desgracias y recordemos un acontecimiento feliz, el del descubrimiento de la estructura de la molécula de benceno.
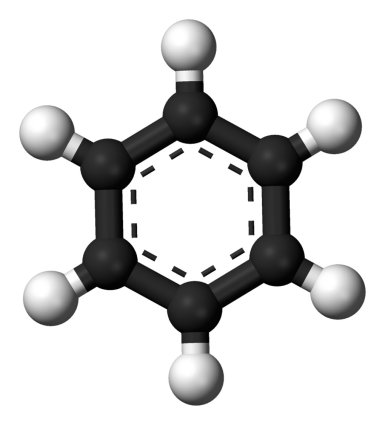
El benceno, como sabemos ahora, es un hidrocarburo cuya molécula tiene la forma de un hexágono plano, con seis carbonos unidos entre sí por enlaces sencillos y dobles alternados -en realidad experimentan un fenómeno denominado resonancia electrónica, pero no es necesario profundizar en este punto- y cada uno de ellos con otros tantos hidrógenos que forman una a modo de corona alrededor del anillo. Del benceno deriva toda una familia de compuestos que por razones históricas se denominan hidrocarburos aromáticos, y los anillos bencénicos revisten una gran importancia en diferentes campos de la química orgánica, desde los hidrocarburos o los polímeros hasta multitud de moléculas bioquímicas.
Pero a mediados del siglo XIX la situación era muy distinta. Se sabía que su fórmula química era C6H 6 y se conocían sus propiedades físicas y químicas, pero la forma de colocar esos doce átomos en una molécula se convirtió en un quebradero de cabeza para los químicos, ya que ninguna de las estructuras que se planteaban conseguía encajar con los resultados experimentales.
Uno de estos químicos era August Kekulé, un científico alemán que previamente había estudiado la tetravalencia del carbono, es decir su capacidad de enlazarse con hasta otros cuatro átomos, así como la de poder hacerlo consigo mismo formando cadenas. Pero la estructura de la molécula de benceno se le resistía también a él.
 |
 |
|
Uróboros (izquierda) y modelo de la molécula de benceno (derecha) |
|
Hasta que un día... la historia, aunque suena fantástica, fue contada por él mismo. Kekulé llevaba tiempo dándole vueltas al rompecabezas, pero seguía sin poder encajar todas las piezas. Hasta que un día, a principios de 1862, se quedó adormilado y tuvo la ensoñación de una serpiente mordiéndose la cola, un símbolo mitológico y alquímico conocido como Uróboros que representa el ciclo eterno.
Pese a que en principio no parecería existir vínculo alguno entre esta vieja alegoría y la estructura de un compuesto químico, Kekulé experimentó su particular ¡eureka! de modo que cuando despertó pudo comprobar que una estructura anular encajaba a la perfección con la escurridiza forma de la molécula de benceno. La ciencia había dado un nuevo paso.
¡Yo llegué primero!
 |
 |
|
Newton (izquierda) y Leibnitz (derecha) |
|
En la historia de la ciencia no resulta infrecuente que dos personas distintas lleguen a un mismo resultado de forma prácticamente simultánea y sin contacto entre ellos. Esto ocurrió, entre otros casos, con el desarrollo de la tabla periódica por Dimitri Mendeleiev y Julius Meyer; el cálculo matemático de la órbita de Neptuno por Urbain Le Verrier y John Couch Adams; el desarrollo de la Teoría de la Evolución por Charles Darwin y Alfred Russel Wallace; la hipótesis de la existencia de un cinturón de cuerpos transneptunianos -el Cinturón de Kuiper- postulada por Kenneth Edgeworth y Gerard Kuiper... sin olvidar las múltiples controversias que surgieron por la primacía en la identificación de un buen puñado de elementos químicos.
Pero existe un caso en que la cosa fue a mayores por razones extracientíficas: el descubrimiento del cálculo infinitesimal, una poderosa herramienta matemática que posibilitó unos enormes avances en el cálculo matemático y que todos conocimos en nuestros estudios de bachillerato como las derivadas y las integrales.
En la segunda mitad del siglo XVII había dos genios trabajando por separado en este tema: el inglés Isaac Newton y el alemán -aunque entonces Alemania todavía no existía como entidad política- Gottfried Leibniz, ambos polifacéticos y ambos sobrados de ego.
Newton sumaba a su genialidad una mala uva más que considerable -vamos, que era un mal bicho- y acostumbraba a machacar a todo aquel que osara cuestionar sus méritos, tal como le ocurrió al desventurado Richard Hooke, otro notable científico inglés que tampoco era una perita en dulce, a quien vapuleó inmisericordemente por pretender disputarle la primacía del descubrimiento de la Ley de la Gravitación Universal.
En lo que al cálculo infinitesimal respecta, todo parece indicar que se trató de unos trabajos en paralelo, aunque Newton fiel a su estilo no lo estimó así; según él lo había desarrollado con anterioridad a Leibnitz pero no publicó sus resultados hasta 1693, mientras Leibnitz empezó más tarde pero lo hizo en 1684.
Aunque en principio lo que contaba era la fecha de publicación y por lo tanto la primacía correspondía a Leibnitz, Newton le acusó de plagiar sus ideas camuflándolas bajo una notación diferente a la de su rival inglés. La guerra estaba declarada, y dada la talla de los contendientes ambos contaron con sus respectivos defensores. Para complicar más la polémica habían intercambiado información en el pasado, por lo que resulta difícil, incluso ahora, determinar cuanto hubo de, digamos, influencia mutua en sus respectivas investigaciones, lo que quizá pudiera haber dado pistas a Leibnitz.
Tras una aparente tregua la guerra se volvió a enconar a principios del siglo XVIII, y en ella llegó a meter baza otro peso pesado de la época, el suizo Johann Bernoulli, que defendió a Leibnitz -o mejor dicho atacó a Newton- para cabreo de este último. En esas estaban, con las derivadas y las integrales convertidas en un conflicto internacional, cuando en 1716 falleció Leibnitz, al que su enconado rival sobreviviría algo más de diez años.
Y no, aquí no se cumplió el refrán de muerto el perro se acabó la rabia, puesto que los partidarios de Newton siguieron despellejando post mortem al difunto Leibnitz, convirtiéndose la polémica en un trasunto político o, mejor dicho, nacionalista de ingleses contra alemanes.
En cualquier caso, y por encima del juego sucio que pudiera haber mediado entre ellos -Leibnitz tampoco era un angelito-, en la actualidad se considera a ambos codescubridores del cálculo diferencial.
Radares y chocolatinas

Horno de microondas
Serendipia es un término inglés, sorprendentemente aceptado por la RAE, que según la definición de su Diccionario, significa “hallazgo valioso que se produce de manera accidental o casual”. A mí me parece, discrepando con los ilustres académicos, que se trata de uno de tantos barbarismos innecesarios ya que disponemos de la tradicional expresión de chiripa, que viene a significar lo mismo y además es igual de larga -cuatro sílabas contando la preposición- que su hispanización, mientras en su idioma original serendipity tiene todavía una más; lo cual desmiente la presunta justificación de que los términos ingleses desplazan a los españoles por ser más cortos y sintéticos.
Pero, mucho me temo, la batalla frente a la papanatería está por desgracia perdida, así que será mejor dejarse de disquisiciones lingüísticas e ir al grano: los descubrimientos casuales que acaban en resultados útiles no buscados ni esperados. Y, aunque la lista es larga, ahora voy a abordar el caso de uno de los electrodomésticos más comunes, el horno de microondas.
Todo empezó cuando durante la II Guerra Mundial se desarrolló el radar -a diferencia del anterior este neologismo anglosajón sí es aceptable, puesto que no existía un término español equivalente- como sistema de detección de los barcos y los aviones enemigos. Aunque ya se conocían con anterioridad los principios básicos de su funcionamiento, como ha ocurrido en tantas otras ocasiones fue necesario un conflicto bélico para acelerar su perfeccionamiento. Y aunque ambos bandos conocían su potencialidad, serían los aliados quienes se adelantaron llevándose el gato al agua.
Tras la finalización de la guerra el radar siguió utilizándose con fines militares, pero también se le encontró un uso civil para la navegación aérea y marítima, sin el cual éstas no habrían alcanzado la importancia que tienen ahora.
Como es sabido, el radar consiste en un emisor de ondas de radio, en el rango de las microondas, asociado a un receptor, la característica antena parabólica. El emisor, llamado técnicamente magnetrón, emite un haz de microondas que al tropezar con un objeto es reflejado rebotando hacia el receptor, que lo señala en una pantalla.
Hasta aquí, me dirán, nada de esto tiene que ver con los hornos de microondas; pero es ahora cuando entra en juego la chiripa. Cuenta la historia que en 1945 Percy Spencer, un ingeniero norteamericano, estaba trabajando con un radar cuando descubrió que una chocolatina que llevaba en el bolsillo se había derretido. Tras varios ensayos descubrió que la emisión de microondas en esas frecuencias calentaba los alimentos, con lo cual el horno de microondas quedó inventado.
La razón de que ocurra este fenómeno se debe a que las microondas provocan la vibración de las moléculas de agua, lo que causa su calentamiento. Puesto que la materia orgánica contiene mucha agua, este calentamiento se extiende al conjunto de los alimentos como podemos comprobar cotidianamente en nuestro propio hogar, dándose la circunstancia de que, a diferencia de las cocinas convencionales de gas o eléctricas, el calentamiento no es externo, sino interno.
Percy Spencer quizás corrió el riesgo -no conozco las condiciones exactas del experimento- de que al calentamiento de la chocolatina le acompañara el de su propio cuerpo. En cualquier caso, si se fijan en el cristal de la puerta verán que cuenta con un enrejado metálico -una plancha con agujeritos- cuya misión es ejercer de filtro para evitar que las microondas generadas por el magnetrón puedan salir del horno provocando potenciales accidentes, por lo cual son absurdas esas manías -conozco algún caso- de no querer utilizarlo porque podría provocar cáncer... cuando lo que provocaría en todo caso serían quemaduras internas. Pero no hay peligro, y por esta misma razón sólo se puede encender con la puerta cerrada para evitar que un despistado se pudiera dejar la mano dentro.
Los rayos que no eran

René Blondlot
En 1903, ocho años después de que Wilhelm Röntgen descubriera los rayos X, el físico francés René Blondlot anunció el descubrimiento de otro tipo de radiación que bautizó con el nombre de rayos N en reconocimiento a la universidad en la que trabajaba, la de la ciudad francesa de Nancy. Los rayos N eran una misteriosa radiación -tan misteriosa como los rayos X entonces- que pronto llamó la atención de los investigadores, dado que aparentemente estaban en todos los sitios; aunque Blondlot los generaba calentando hasta la incandescencia en un alambre de platino encerrado en un tubo de hierro cerrado por una lámina de aluminio que oficiaba de ventana, se comunicó el descubrimiento de emisiones de rayos N en el Sol, en varios minerales, en el agua marina e incluso en los músculos, los nervios y hasta en el cerebro.
Los omnipresentes rayos N presentaban una serie de peculiaridades llamativas: excitaban una llama de gas o una pantalla de sulfuro de calcio, atravesaban los metales y prácticamente cualquier sustancia opaca, aumentaban la agudeza visual, potenciaban la acción de los fármacos, interaccionaban con los anestésicos...
Tan bonita resultaba la historia que proliferaron los artículos que avalaban su descubrimiento. 120 científicos algunos tan prestigiosos como Henri Becquerel, descubridor de la radiactividad, Henri Poincaré y Arsène d'Arsonval lo apoyaron sin fisuras, e incluso surgieron varios pretendientes que reclamaron la prioridad del descubrimiento. Tal fue el delirio, que en 1904 la Academia de Ciencias Francesa otorgó su prestigioso premio Lecont a Blondlot dejando fuera nada menos que al mismísimo Pierre Curie.
Pero la realidad se mostró cruel. Pronto comenzaron a ser muchos, tanto en Francia como sobre todo en otros países, los que manifestaron su escepticismo acerca de la naturaleza de los rayos N, principalmente porque no lograban repetir los resultados de Blondlot, algo fundamental en la investigación científica. Quien finalmente demostró que los rayos N no existían fue el físico norteamericano Robert Williams Wood, experto en varios campos y principalmente en el estudio de la radiación ultravioleta. Wood no acusó a Blondlot de farsante, defendiendo su buena fe pero acusándole de falta de rigor experimental y de haberse autoengañado con su presunto descubrimiento, siendo su ayudante quien cargó con las sospechas de haber actuado de manera fraudulenta. En cualquier caso Blondlot quedó desacreditado como científico y murió olvidado en 1930.
Aunque desde el punto de vista científico no hay mucho más que decir, existe un factor externo que conviene considerar. Tras la humillante derrota francesa de 1870 en la guerra franco-prusiana, Francia y Alemania mantuvieron una rivalidad total que acabó derivando en la I Guerra Mundial dentro del marco de los exacerbados nacionalismos que surgieron, no sólo en estos dos países, en esa época. El resentimiento francés no se limitó al ámbito político y militar, abarcando otros como el cultural -basta con leer la novela de Julio Verne Los quinientos millones de la Begún- o el científico, donde el sonado descubrimiento de los rayos X por el alemán Röntgen habría encontrado su contrapartida en los ficticios rayos N, para satisfacción del orgullo francés, incluyendo con toda probabilidad al propio Blondlot. Porque, como es de sobra sabido, los nacionalismos ciegan.
El descubrimiento de Neptuno

Neptuno, fotografiado por la sonda Voyager 2
En el siglo XIX la astronomía experimentó un gran desarrollo apoyada en dos puntales: los telescopios cada vez más perfeccionados y potentes, y las matemáticas que desarrollando la teoría gravitatoria de Newton llegaron a un grado de sofisticación que permitía calcular las órbitas de los planetas, satélites y otros cuerpos menores del Sistema Solar con una precisión si precedentes.
Así pues, no es de extrañar que ya en 1821, cuatro décadas después del descubrimiento de Urano y cuando éste había recorrido aproximadamente la mitad de su órbita, los astrónomos descubrieron discrepancias entre sus cálculos y la trayectoria real del planeta. La suposición que manejaron fue la posible existencia de un planeta exterior a Urano cuya atracción gravitatoria alteraría la trayectoria de éste, por lo que procedieron a su búsqueda.
Sin embargo, desde un punto de vista estricto Neptuno no fue descubierto, sino calculado. O, más concretamente, lo fueron su órbita y el lugar de ella en el que se encontraría en un momento dado. Quien se encargó de hacerlo fue el matemático inglés John Couch Adams, que mandó sus resultados al astrónomo real George Airy, quien le solicitó más datos que Adams, según cuentan las crónicas, no le llegó a enviar.
 |
 |
|
John Couch Adams (izquierda) y Urbain Le Verrier (derecha) |
|
Este retraso sería fundamental para que otro matemático, el francés Urbain Le Verrier, realizara sus propios cálculos de manera independiente, publicándolos el 31 de agosto de 1846 y adelantándose a Adams en dos días. El 18 de septiembre de ese mismo año Le Verrier envió sus resultados al astrónomo alemán -esto ocurrió 24 años antes de la derrota francesa de 1870- Johann Galle, el cual la misma noche del día en el que le llegó la carta, el 23 de septiembre, descubrió Neptuno a tan sólo un grado de distancia -aproximadamente el doble del diámetro de la luna llena- del punto calculado por Le Verrier, bastante más preciso que el determinado por Adams.
El triunfo del modelo matemático para calcular órbitas animó a los astrónomos a aplicarlo en otros casos en los que también se apreciaron anomalías, aunque los resultados fueron dispares. Mercurio presentaba un comportamiento similar, por lo que Le Verrier propuso en 1859 la existencia de un planeta más cercano al Sol al que bautizó con el nombre de Vulcano. Tanto Le Verrier como otros astrónomos se aplicaron a la tarea, siendo varias las comunicaciones del descubrimiento de Vulcano pese a la dificultad de observar las regiones cercanas al Sol donde teóricamente debía orbitar. Finalmente los astrónomos acabaron aceptando la inexistencia del escurridizo planeta, pero no sería hasta 1915 cuando la Teoría de la Relatividad explicó las perturbaciones de la órbita de Mercurio a causa de la atracción gravitatoria del Sol.
El caso del descubrimiento de Plutón es más complejo, ya que se trató de una chiripa científica. A finales del siglo XIX se descubrió que la existencia de Neptuno no bastaba para explicar la totalidad de las irregularidades de la órbita de Urano, por lo que se postuló la posible existencia de un planeta transneptuniano. Unos años después, en 1906, Percival Lowell, en colaboración con William Pickering , iniciaron la búsqueda del que denominaron Planeta X en el lugar donde indicaban los cálculos. Aunque años después se encontraron varias fotografías que recogían su existencia, en ese momento no supieron identificarlo confundiéndolo con una estrella lejana.
Hubieron de pasar dos décadas hasta que el 13 de marzo de 1930 Clyde Tombaugh, un joven astrónomo que trabajaba en el observatorio fundado por Lowell, descubrió oficialmente al planeta que sería bautizado con el nombre de Plutón. En un principio se pensó que Plutón sería el responsable del resto de las perturbaciones ajenas a Neptuno, pero como no se le conocía ningún satélite no se pudo determinar su masa a partir del radio y el período orbital de éstos, por lo que ésta se estimó en base a la cantidad necesaria para justificar estas perturbaciones, dando como resultado un valor de magnitud similar a la de la Tierra aunque su lejanía impedía realizar cálculos más precisos.
No obstante, otras observaciones posteriores parecieron indicar que Plutón debía tener un tamaño menor. La confirmación a estas sospechas llegó cuando en 1978 James W. Christy descubrió Caronte, el primero de los cinco satélites que se le conocen ahora, y el de mayor tamaño; de hecho algunos astrónomos consideran al sistema Plutón-Caronte como un planeta binario. La existencia de Caronte permitió calcular la masa y el tamaño de ambos, que en 2015 confirmaría la sonda New Horizons.

Plutón (derecha) y Caronte
(izquierda) fotografiados por la sonda New Horizons
Plutón resultó ser más pequeño de lo que se pensaba, menor incluso que la Luna ya que su diámetro es de tan sólo 2.370 kilómetros, apenas un 70% del lunar, y su masa es todavía menor dado que su densidad es de 1,75 gramos por centímetro cúbico frente a los 3,34 de nuestro satélite y los 5,51 de la Tierra. Caronte es todavía menor, con un diámetro de 1.208 kilómetros y una densidad de 1,65 g/cm3. Dadas sus reducidas dimensiones, en 2006 Plutón fue degradado a la categoría de planeta enano.
En resumen, ni siquiera considerando la masa conjunta de Plutón y Caronte -las de los restantes satélites son insignificantes- se justifican las anomalías orbitales de Urano que motivaron su descubrimiento, el cual se debió en realidad a una afortunada casualidad. Por si fuera poco el descubrimiento a partir de 1992 de numerosos cuerpos similares orbitando más allá de Neptuno, los transneptunianos, ha demostrado que Plutón es tan sólo uno más de ellos, algunos de tamaño similar al suyo pero ninguno que pueda ser considerado planeta.
Esto no ha frenado las teorías de la posible existencia de uno o más planetas en las regiones remotas del Sistema Solar, pero al día de hoy no existen indicios fehacientes de su presencia.
El escurridizo teorema de Fermat

Pierre de Fermat
Pierre de Fermat fue un matemático francés, nacido en 1601 y fallecido en 1665, al que se le considera uno de los mejores matemáticos de su época junto con Descartes y Kepler. Fueron varias las aportaciones que se le deben en campos tales como la teoría de probabilidades, la geometría analítica o la teoría de números, pero es más conocido por el gran público por el denominado último teorema de Fermat, llamado así porque es uno de los varios que llevan su nombre. Éste es su enunciado:
Siendo n un número entero mayor que 2, no existen números enteros positivos x, y, z con los que se cumpla la igualdad:
xn + yn = zn
Puesto que las definiciones matemáticas suelen resultar engorrosas para los profanos, entre los que me incluyo, voy a intentar explicarlo de una forma más sencilla. Los números enteros son aquéllos que carecen de decimales, y positivos los mayores de cero. Empezando por el primer número entero positivo, el 1, nos encontramos con un caso trivial puesto que un número elevado a 1 conserva el mismo valor, con lo cual la ecuación se convierte en una simple suma del tipo x+y=z.
Con n=2 la ecuación se convierte en el teorema de Pitágoras que todos estudiamos en el colegio:
x2 + y2 = z2
Cuya conocida definición geométrica afirma que en un triángulo rectángulo la suma de los cuadrados de los catetos es igual al cuadrado de la hipotenusa. El teorema de Fermat introduce una restricción, la de que tanto los dos catetos como la hipotenusa sean números enteros, y basta con un simple cálculo para demostrar que hay casos en lo que sí existe una solución entera para z, como por ejemplo:
32 + 42 = 52
O lo que es lo mismo, 9+16=25. No siempre ocurre así, puesto que en este otro ejemplo:
22 + 32 = z2
Tenemos que z2=4+9=13, cuya raíz cuadrada no es un número entero sino el irracional 3,60555...
El teorema de Fermat exige que no exista ningún caso en el que se pueda resolver la ecuación con valores enteros para las tres variables, pero como acabamos de comprobar con n=2 para el exponente sí es posible encontrar valores de x, y, z con los que la ecuación se cumple. Tal como está redactado el teorema basta con una sola discrepancia para que resulte falso, razón por la que Fermat excluyó el 2.
La cuestión se complica si pasamos al siguiente valor de n, el 3, para el cual el teorema de Fermat sí resulta aplicable o, si se prefiere, la ecuación no tiene ninguna solución, sean cuales sean los valores de las tres variables siempre dentro de los números enteros:
x3 + y3 = z3
Que ya no se puede aplicar a un triángulo rectángulo, puesto que los exponentes cúbicos corresponden no a superficies, sino a volúmenes tridimensionales. Para valores mayores de 3 nos quedamos sin el auxilio de la geometría clásica siendo necesario recurrir a las geometrías multidimensionales, algo que está al alcance tan sólo de matemáticos especializados en este campo.
Así pues, la aparente sencillez del teorema esconde una endiablada dificultad. De hecho no pudo ser demostrado hasta 1995, más de tres siglos y medio después de que Fermat lo planteara hacia 1637 escribiéndolo como al descuido en el margen de un libro, añadiendo el muy cuco que había desarrollado la demostración pero no le cabía allí. Con dos narices.
Conviene insistir en que para que un teorema matemático quede demostrado ha de probarse que se cumple en la totalidad de los casos en los que es aplicable -en este caso los números naturales- sin ninguna excepción, y nadie hay más tajante entre los científicos que los matemáticos a la hora de exigir una demostración, mientras que los que no lo somos solemos conformarnos con un “casi siempre” asumiendo que no resulta posible abarcar la totalidad de los parámetros que afectan a un fenómeno real.
Así pues, reconozco que soy incapaz de comprender las sutilezas matemáticas de este teorema, por lo que me limitaré a reseñar su varias veces centenaria historia. Fermat falleció en 1665, casi 30 años después de plantearlo, por lo que tuvo tiempo de sobra para escribir la demostración usando todo el papel que necesitara; pero por las razones que fueran no lo hizo, llevándose la solución a la tumba. Y como la famosa anotación no se descubrió hasta después de su muerte, tampoco hubo oportunidad de preguntárselo. Tan sólo dejó una demostración para el caso particular de n=4, lo cual si bien desbrozaba el terreno al permitir descartar los números que no son primos, dejaba pendiente de demostración su cumplimiento para los números primos. Les ruego que no me pidan que se lo explique, porque no lo entiendo y me limito a repetirlo.
Y así quedó la cosa, con el dichoso teorema convertido en uno de los problemas pendientes más famoso -y también más enrevesado- de la historia de las matemáticas. Pero como los matemáticos son por naturaleza cabezotas, se empeñaron en resolverlo convirtiendo la conjetura -así denominan a los teoremas pendientes de resolución- en un teorema en firme... con modestos resultados, puesto que hasta mediados del siglo XIX, es decir, durante los dos siglos siguientes, tan sólo lo lograron para los tres primeros números primos, a excepción del 1 y el 2, que quedaban fuera de la definición: el 3, el 5 y el 7. Lo cual no se puede decir que fuera demasiado teniendo en cuenta el enorme desarrollo que experimentaron las matemáticas a lo largo de esos años.
A partir de entonces se siguieron haciendo avances con pruebas mucho más complejas que, si bien ampliaban el conjunto de números para los que el teorema se cumplía, seguían dejando fuera a muchos más... y recordemos que la cantidad de números primos es infinita. Incluso utilizando ordenadores, y ya entramos en la segunda mitad del siglo XX, tan sólo se llegaron a probar hasta cuatro millones de números primos. Ya en fechas tan recientes como la década de 1980 los avances matemáticos en otros campos abrieron nuevas vías que permitieran demostrar que ninguno de los infinitos números primos invalidaba el teorema. Finalmente sería el matemático inglés Andrew Wiles quien logró vencer los últimos obstáculos proponiendo en 1993 una demostración del teorema que, tras una revisión, alcanzó su versión definitiva en 1995.
Yo, lo reconozco, no habría tenido tanta paciencia.
Otra muerte evitable

Henry Moseley
Volvemos a la cara oscura de la historia de la ciencia para recordar un caso hasta cierto punto similar al de Galois, aunque las circunstancias fueron diferentes y en éste no hubo temeridad alguna por parte del afectado, aunque quizás sí por sus superiores, saldado también con la pérdida de su vida.
Me estoy refiriendo a Henry Moseley, uno de los más importantes físicos de principios del siglo XX y eso que estamos hablando de científicos de la talla de Einstein, Rutherford, Bohr, Heisenberg, Planck, Schödringer, Pauli, Dirac, de Broglie o Fermi, entre muchos otros. Pero antes de esbozar una pequeña biografía de Moseley, resulta necesario retroceder unas cuantas décadas para disponer de la necesaria perspectiva histórica.
A mediados del siglo XIX los químicos habían descubierto un considerable número de elementos químicos, pasando de los 33 conocidos en 1800 a los 59 de 1850, planteándose el problema de su clasificación. Se sabía que algunos de ellos presentaban propiedades químicas y físicas parecidas, como era el caso del litio, el sodio y el potasio, o el del flúor, el cloro y el bromo; pero aunque se habían hecho algunos intentos parciales se estaba lejos de encajar todas las piezas y, por si fuera poco, los nuevos descubrimientos lo complicaban todavía más.
El acierto de organizarlos en una única tabla, que recibió el nombre de periódica dado que las propiedades de los elementos se repetían periódicamente le correspondió al químico ruso Dimitri Mendeleiev, aunque su figura oscurece al alemán Lothar Meyer que también desarrolló la suya de forma paralela publicándola tan sólo un año después.
Para hacerlo Mendeleiev se basó en una propiedad de los elementos que ya se conocía con suficiente precisión, la masa atómica, aunque todavía se estaba lejos de conocer la estructura de los átomos. Lo que hizo ahora nos parece sencillo, pero entonces supuso una enorme intuición: tomó los 63 elementos conocidos y empezando por el elemento más ligero, el hidrógeno, los fue colocando en una fila horizontal en orden creciente de masas atómicas. Cuando comprobaba que las propiedades químicas se repetían, saltaba a una fila inferior comenzando por el principio, de manera que los elementos químicos con propiedades afines formaban columnas verticales a las que llamó familias.
El método funcionó bastante bien y de hecho la tabla de Mendeleiev es, con algunas modificaciones, la misma que empleamos ahora. No obstante se vio obligado a resolver dos cuestiones que se le plantearon, el de los elementos que todavía no habían sido descubiertos, que solucionó dejando los huecos vacíos, y los casos en los que en la ordenación por masas atómicas quedaban pares de elementos cambiados, que se limitó a invertir.
El resultado final era completamente funcional y permitió la inclusión de los nuevos elementos descubiertos con posterioridad, por lo que la tabla periódica fue adoptada sin problemas por los químicos. Pero a los físicos no acababa de gustarles su naturaleza empírica, por lo que deseaban encontrar una explicación teórica que además evitase la necesidad de introducir excepciones. Ésta llegaría con el desarrollo de los modelos atómicos que describían su estructura interna, pero el primero de ellos, el de Bohr, data de 1913 y no dejó de ser una primera aproximación, mientras el modelo cuántico, que es el actual, fue propuesto por Schrödinger en 1926. Esto sin contar con que las partículas subatómicas también tardaron bastante en ser identificadas: el electrón fue el primero en 1897, el protón en 1918 y para el neutrón hubo que esperar hasta 1932.
Así pues, a principios del siglo XX seguía sin conocerse una interpretación teórica de la tabla periódica; y es ahora cuando entra en escena nuestro biografiado. Henry Moseley había nacido en 1887 y recibió una esmerada educación, siendo alumno del afamado Ernest Rutherford. Pronto destacó en sus investigaciones y en 1913, con apenas 26 años, definió el número atómico, que reemplazó a la masa atómica en la ordenación de la tabla periódica, pudiéndose interpretar ésta al fin de forma teórica.
El trabajo de Moseley consistió en analizar los espectros de rayos X de una cincuentena de elementos químicos, descubriendo que todos ellos contaban con un registro específico que los diferenciaba del resto; en lenguaje coloquial podríamos decir que estos espectros constituían el equivalente a su huella dactilar o al número de DNI.
Aún más, determinó que existía una relación entre la raíz cuadrada de la frecuencia del pico principal, denominada Ka, del espectro y el número atómico del elemento, definido este último como el número de orden de la casilla que le corresponde en la tabla periódica. Es la denominada Ley de Moseley, que permitía además identificar a un elemento en una muestra desconocida midiendo la frecuencia principal de su espectro de rayos X y calculando el número atómico a través de la ley.
Ahora sabemos que el número atómico corresponde al número de protones existentes en el átomo y que es el que determina las propiedades químicas del mismo, pero entonces todavía no se había descrito al protón y la estructura atómica estaba todavía en mantillas. Con toda probabilidad Moseley habría seguido investigando sumando sus trabajos a todos aquellos estudios que acabaron permitiendo el desarrollo de la mecánica cuántica, pero la fatalidad se atravesó en su vida.
Tras el estallido de la I Guerra Mundial se alistó en el ejército británico -el servicio militar obligatorio no se introdujo en Gran Bretaña hasta enero de 1916-, siendo destinado a una de las unidades que intervinieron en la batalla de Galípoli, una carnicería en la que tan sólo los británicos sufrieron 250.000 bajas; entre ellas la de Moseley, muerto el 10 de agosto de 1915 sin llegar a cumplir los 28 años.
Sólo podemos aventurar lo que podría haber aportado a la ciencia de no haberse interpuesto una bala en su vida.
Edison, cara y cruz

Thomas Alva Edison
Thomas Alva Edison (1847-1931) es uno de los iconos de la ciencia y la ingeniería norteamericanas, así como símbolo del modelo de norteamericano hecho a sí mismo a partir de la nada. De hecho careció no sólo de estudios universitarios sino de una formación docente normal, siendo su talento el que le llevó a convertirse en uno de los inventores más famosos no sólo de su país, sino de todo el mundo.
Las cifras dan buena muestra de su valía: registró a su nombre más de mil patentes, y se le reconoce como el inventor, o cuanto menos el desarrollador, de tecnologías tales como las redes de luz eléctrica, la lámpara incandescente, el fonógrafo, las baterías eléctricas o el kinetoscopio -un antecedente del cine-, entre los más conocidos.
Asimismo Edison fue un empresario de éxito convirtiéndose en millonario, otro de los mitos norteamericanos que identifica talento con triunfo económico, lo cual dicho sea de paso resulta discutible; aunque en este caso sí se cumplió.
Sin embargo la imagen mitificada de Edison, reflejada en dos famosas películas rodadas en 1940 -El joven Edison y Edison, el hombre-, y sus innegables méritos, no pueden ocultar la cruz del prolífico inventor y exitoso empresario, mucho menos luminosa que su biografía oficial. Porque Edison fue también un empresario rapaz y sin escrúpulos que no dudaba en apropiarse de inventos ajenos o en recurrir a métodos discutibles para imponerse ante sus rivales.
Aparte de que también cometió errores, algunos de bulto como su conocido empecinamiento en utilizar corriente continua en las incipientes redes de distribución de luz eléctrica, pese a las evidencias -y la demostración de Nikola Tesla- de las ventajas de hacerlo con corriente alterna. Lo que no evitó que se enzarzara en una guerra comercial con la compañía Westinghouse Electric, partidaria de la corriente alterna y en la que recaló Tesla tras su brusca salida de la compañía de Edison.
Ya que he citado a Tesla conviene recordar que este genial ingeniero checo llegó a estar contratado por Edison, pero acabó abandonando su empresa con cajas destempladas; no se sabe muy bien lo que ocurrió, pero se especula con que Edison o sus gerentes maltrataron a Tesla, e incluso se insinúa que Edison pudiera haberse aprovechado de sus descubrimientos en beneficio propio.
Edison no tenía escrúpulos a la hora de sacar rendimiento económico a sus inventos, muchos de los cuales no eran en realidad suyos sino modificaciones o ensayos sobre otros ya existentes, pero que patentaba a su nombre. Éste fue el caso de la lámpara incandescente, que no inventó pero sí perfeccionó mediante una mejora del material del filamento.
Caso aparte es la invención en 1895 del cinematógrafo por los hermanos Lumière. Edison había creado un año antes el kinetoscopio, al que se puede considerar como un precursor del cine, y a partir de éste desarrolló el vitascopio. No fueron éstos los únicos intentos de perfeccionar el nuevo invento, pero el problema surgió cuando Edison patentó a su nombre el cinematógrafo litigando primero con los Lumière, que vieron frenada su expansión en los Estados Unidos a causa de la imposición de leyes proteccionistas, y posteriormente por su pretensión de detentar el control de los derechos de explotación en los Estados Unidos.
No contento con querer cobrar por la exhibición de cualquier película, pretendió también hacerlo con la venta de cámaras, proyectores y hasta de la película virgen, pese a que ésta había sido inventada por George Eastman, el fundador de la conocida compañía Kodak, y él sólo introdujo la innovación de las perforaciones laterales para arrastrarla. Se trataba claramente de apropiaciones arbitrarias y abusivas, pero ante la perspectiva del dinero que podrían generar, y en esto no se equivocó, sobraban los escrúpulos y bastaban los abogados.
Quienes pagaron el pato de la codicia de Edison fueron los productores independientes que habían empezado a surgir en Nueva York, desarrollándose la disputa no sólo en el plano legal sino también con coacciones por parte de los detectives, o matones según se interprete, contratados por Edison. La solución fue drástica: los productores emigraron en masa a California, justo al otro extremo del país, asentándose en lo que entonces era un pequeño poblado llamado Hollywood. Un sitio ideal no sólo por su aislamiento y buen clima para los rodajes, sino también porque estaba suficientemente lejos de los abogados y los matones de Edison y lo suficientemente cerca de México como para poder poner tierra por medio en caso de necesidad. El resto es historia.
¿Cuándo fueron descubiertos Urano y Neptuno?
 |
 |
|
Urano (izquierda) y Neptuno (derecha) fotografiados por la sonda Voyager 2 |
|
Seguramente se extrañarán ustedes de la pregunta, puesto que bastará con buscar en internet para encontrar la respuesta: Urano fue descubierto por William Herschel el 13 de marzo de 1781 desde la ciudad inglesa de Bath y Neptuno, tal como he comentado anteriormente, lo fue por Johann Galle el 23 de septiembre de 1846 desde el Observatorio de Berlín siguiendo los cálculos matemáticos de Urbain Le Verrier, realizados en paralelo con los de John Couch Adams. Además, del descubrimiento de Neptuno ya he hablado. Así pues, ¿qué tienen de curiosidad estos datos?
Pues la tienen, dado que en realidad tanto el uno como el otro habían sido observados con anterioridad por varios astrónomos. Digo observados, y no descubiertos, puesto que los primeros que los identificaron como planetas fueron efectivamente Herschel y Galle en las fechas y los lugares citados, por lo que a ellos corresponde el honor de sus respectivos descubrimientos; pero tampoco sería justo olvidar a sus predecesores, por más que no llegaran a identificar su naturaleza confundiéndolos con estrellas débiles.
Comencemos por Urano. La observación más antigua que se conoce, casi un siglo anterior a la de Herschel, fue la del astrónomo británico John Flamsteed en 1690, el cual lo catalogó erróneamente como la estrella 34 Tauri. En 1738 el también inglés John Bevis lo registró en tres ocasiones consecutivas, a lo largo de tres meses, como tres estrellas diferentes -obviamente Urano se desplazaba por el firmamento-, que ya fue “afinar”. Por último, entre 1750 y 1769 el francés Pierre Charles Le Monnier lo observó en varias ocasiones. Incluso el propio Herschel lo catalogó inicialmente como un cometa antes de identificar su verdadera naturaleza.
Neptuno también contó con predescubridores, aunque su mayor lejanía y por consiguiente su menor brillo que Urano -su magnitud aparente es de 7,84, frente a 5,52 de aquél- dificultaba su observación para los telescopios de la época. El primero de ellos fue nada menos que Galileo en 1612, y de nuevo en 1613, quien lo localizó con su recién inventado y rudimentario telescopio, apenas dos años después de sus observaciones de la superficie lunar y del descubrimiento de los cuatro satélites principales de Júpiter, confundiéndolo en ambas ocasiones con una estrella. Se dio así la paradoja de que no sólo se adelantó en 234 años al descubrimiento oficial de Neptuno, sino que también lo hizo en 78 años al primer avistamiento de Urano. A la observación de Galileo siguieron las dos del francés Joseph de Lalande en 1795, la de John Herschel -hijo de William Herschel- en 1830 y las tres del astrónomo alemán Johann Von Lamont entre 1845 y 1846.
Un gas “extraterrestre”
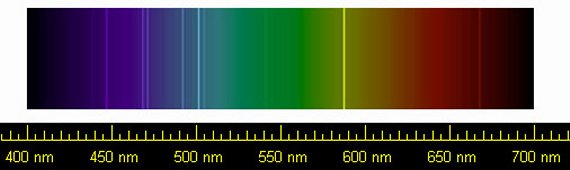
Espectro del
helio
La historia del descubrimiento de los elementos químicos, además de apasionante, daría por sí sola para varios libros... que ya están escritos. Obviamente resultaría excesivo relatarla aquí, pero no puedo evitar la tentación de relatar el caso de uno de ellos por la singularidad que tuvo descubrirlo fuera de la Tierra antes de hacerlo aquí; y no me estoy refiriendo a un hallazgo realizado por la NASA o cualquier otra agencia espacial puesto que tuvo lugar en 1868, mucho antes de que la astronáutica diera sus primeros pasos.
Me estoy refiriendo al helio, el segundo elemento más ligero después del hidrógeno y el que encabeza en la tabla periódica la familia de los gases nobles junto con el neón, el argón, el kriptón, el xenón y el radón. El helio, un gas inerte que no reacciona con ningún otro elemento o compuesto químico, resulta familiar dado que su utilidad más habitual es el llenado de globos, desde los meteorológicos y en su día los dirigibles, hasta los globos de goma con los que juegan los niños, aunque evidentemente tiene otros usos. Su gran ligereza hace que sus átomos asciendan hasta las capas altas de la atmósfera, siendo preferible su uso al del hidrógeno, pese a su menor poder ascensional, dado que evita los riesgos inherentes a la inflamabilidad del hidrógeno.
El helio, tal como he anunciado, no fue descubierto por primera vez en la Tierra, sino en el Sol. Obviamente nadie fue allí a tomar una muestra que pudiera ser analizada en un laboratorio, sino que se descubrió gracias a la espectroscopía. Isaac Newton fue el primero que en 1672 logró desdoblar la luz solar, haciéndola pasar a través de un prisma transparente, en un conjunto de colores similares a los del arco iris, pero no fue hasta 1815 cuando el físico y astrónomo alemán Joseph von Fraunhofer estudió en detalle el espectro solar, es decir la descomposición de la luz solar en sus componentes.
La espectroscopía no tardó en aplicarse a diferentes gases, metales o compuestos químicos en el laboratorio, mostrándose como una técnica de análisis extremadamente útil ya que, como pronto se descubrió, los espectros eran característicos de cada elemento químico, pudiéndose identificar la naturaleza de éstos sin necesidad de realizar análisis químicos en ocasiones complejos e incluso fueron varios los elementos del sistema periódico que se descubrieron mediante técnicas espectroscópicas antes de ser aislados químicamente.
Asimismo importante fue descubrir que gracias al estudio de los espectros luminosos de objetos tan inaccesibles como el Sol, las estrellas o los planetas, se pudieron identificar los elementos que los constituían, ya que éstos eran similares a sus homólogos terrestres. Con el tiempo la espectroscopía se aplicaría también a otros rangos de la radiación electromagnética como el infrarrojo, el ultravioleta o los rayos X, pero este tema se sale de nuestro ámbito.
Pero no todo acababa de encajar. En 1868 el astrónomo francés Pierre Janssen y su colega inglés Norman Lockyer descubrieron por separado unas líneas del espectro solar que no concordaban con las de ningún elemento químico conocido, por lo que postularon la presencia en el Sol de un elemento inexistente en la Tierra que fue bautizado como helio, en homenaje al dios griego Helios que simbolizaba al Sol.
Sin embargo el helio sí existía en la Tierra, aunque no fue descubierto en nuestro planeta hasta 1882, también por métodos espectroscópicos, por el físico italiano Luigi Palmieri. Posteriormente en 1895 el afamado químico inglés William Ramsay logró aislarlo en estado puro extrayéndolo de una variedad de uranita, un mineral de uranio. Por último, ya a principios del siglo XX, se descubrió que el helio existía en estado libre mezclado con otros gases en yacimientos de gas natural, de donde se sigue extrayendo en la actualidad.
El éxito del descubrimiento extraterrestre del helio condujo paradójicamente a otros descubrimientos erróneos. Durante la observación de un eclipse solar en 1869 los astrónomos Charles Augustus Young y William Harkness descubrieron, también por separado, unas líneas desconocidas en el espectro de la corona solar, sólo visible durante los eclipses totales. Siguiendo la línea de sus colegas las atribuyeron a un nuevo elemento químico, al que llamaron coronio en alusión a su procedencia aunque posteriormente sería renombrado como newtonio. No fue sino hasta la década de 1930 cuando se demostró que el espectro del coronio correspondía en realidad a átomos de hierro altamente ionizados, es decir que habían perdido un gran número de electrones en las condiciones extremas de la corona solar, por lo que no existen como tales en la Tierra.
Otro error similar fue el del nebulio, identificado espectroscópicamente en la nebulosa -de ahí su nombre- NGC 6543 Ojo del Gato en 1864, algunos años antes del descubrimiento del helio. El error se perpetuó durante décadas en 1927 se demostró que el espectro correspondía a átomos de oxígeno doble o triplemente ionizados en una condiciones que, como en el caso anterior, no existen en nuestro planeta.
Los canales de Marte

Fotografía de Marte
tomada por el Viking 1 en 1980. No existen los canales,
pero sí el
el largo y profundo cañón del Valles Marineris.
Es de sobra conocida la afirmación de que una mala traducción puede arruinar un texto, pero en pocas ocasiones una palabra traducida equivocadamente pudo causar un error de tanta repercusión como el de la presunta -e inexistente- existencia en Marte de canales excavados por una hipotética civilización marciana, con objeto de conducir la escasa cantidad de agua presente en el planeta desde los polos hasta el resto de la superficie del moribundo -así lo consideraban los astrónomos del siglo XIX y principios del XX- planeta rojo.
Todo empezó cuando el astrónomo italiano Giovanni Schiaparelli comunicó en 1877 el descubrimiento de una red de “canales” recorriendo la superficie del planeta, aunque nunca afirmó que fueran artificiales ni los dibujó rectilíneos, atribuyéndoles un origen geológico. Quien propaló su presunta naturaleza artificial fue el estadounidense Percival Lowell que, con independencia de su innegable talla científica, tenía una irreprimible tendencia hacia lo que hoy denominaríamos magufismo. En consecuencia, y dado su prestigio, se desató una martemanía en la que otros astrónomos creyeron ver también los canales, llegando a dibujarse unos completos mapas de la superficie marciana en los que se reflejaban sus trazados inequívocamente rectilíneos.
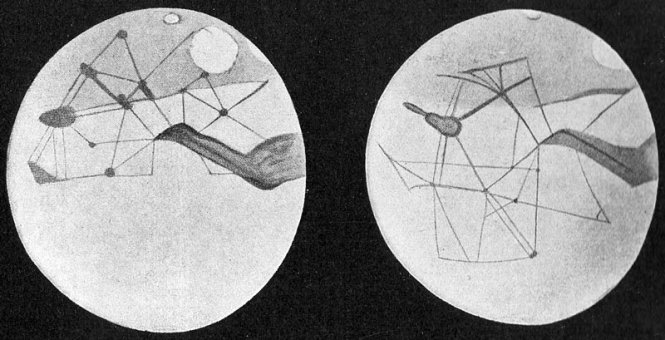
Los presuntos canales marcianos
dibujados por Percival Lowell. Ilustración tomada de la
Wikipedia
Observaciones posteriores más detalladas y con telescopios más precisos de otros astrónomos, entre ellos el español José Comas Solá, pusieron en duda la existencia de estos canales artificiales, argumentando que en realidad se trataba de accidentes geográficos de índole natural. Con el tiempo se confirmaría que ésta era la teoría correcta, y las sucesivas misiones espaciales enviadas a Marte demostraron la inexistencia de estos “canales” aunque sí encontraron antiguos cauces excavados por ríos hoy desaparecidos, algunos de enorme magnitud como el impresionante Valles Marineris. No obstante, la romántica idea de un planeta moribundo surcado por canales excavados por sus extintos -o todavía supervivientes- habitantes tendría un hondo calado en la ciencia ficción aun mucho después de que hubiera sido descartada por los astrónomos.
El error, magnificado por la tozudez de Lowell, estuvo provocado por lo que los profesores de idiomas denominan falsos amigos, palabras similares en dos lenguas que, sin embargo, tienen significados distintos. Error, por cierto, que no habría sido posible en español puesto que nosotros disponemos de dos palabras diferentes para definir los cursos naturales de agua -cauces- y los artificiales -canales-, aunque existen algunas excepciones como el Canal de la Mancha o el Canal Beagle, en el extremo sur del continente americano.
En otros idiomas, por lo que he podido indagar aunque disto mucho de tener soltura con las lenguas extranjeras, la situación suele ser más o menos similar, pero el problema radica tal como he comentado en las traducciones. Schiaparelli utilizó el término italiano “canali”, que en esta lengua no tiene la connotación de cauce artificial, pero al traducirse al inglés en lugar de escribir “channels”, que tiene un significado similar al español “cauces”, se hizo con “canals”, equivalente a nuestro “canales”. Con lo cual la confusión y el afán de Percival Lowell hicieron el resto.
El mejor escribano echa un borrón

Y sin embargo, vuelan.
Fotografía tomada de
www.iberia.com
Una de las virtudes del método científico es su capacidad de rectificar cuando una teoría resulta errónea, lejos del dogmatismo de otras escuelas de pensamiento. Pese a ello los cambios no siempre se producen con la conveniente rapidez y, ya a título individual, existen en la historia de la ciencia casos de meteduras de pata garrafales por parte de científicos justamente renombrados.
Uno de los más llamativos es el de William Thomson, más conocido como lord Kelvin, uno de los más importantes científicos de finales del siglo XIX. Son de sobra conocidas sus aportaciones en diversos campos de la ciencia como la termodinámica -fue él quien definió el cero absoluto de temperatura proponiendo una escala de temperaturas conocida con su nombre-, la electricidad o la ingeniería, colaborando en la instalación del primer cable telegráfico trasatlántico.
Justamente respetado y considerado en su época acumuló nombramientos y homenajes, lo que no impidió que cometiera errores tan garrafales como cuando en 1895 declaró tajantemente que era imposible que los aviones pudieran volar y en 1902 predijo que ningún globo ni avión tendrían éxito. Apenas un año después, en 1903, dos fabricantes de bicicletas sin conocimientos científicos, los hermanos Wright, realizaron el primer vuelo de la historia en su tosco aparato, y pocos años más tarde los aviones eran una realidad.
También se columpió afirmando en 1895 ese mismo año que los rayos X eran un engaño, aunque posteriormente se retractaría; en 1897 que la radio no tenía futuro y en 1898 que el oxígeno del planeta se agotaría en tan sólo cuatro siglos a causa de la quema de combustibles. Sin olvidar tampoco que en su juventud entró en contradicción con Darwin y los geólogos al postular que la edad de la Tierra oscilaba entre los 24 y los 100 millones de años.
Y es que, como dice el refrán, el mejor escribano echa un borrón... o varios.
Cuestión de pegajosidad

Taco de notas post-it.
Fotografía tomada de la
Wikipedia
Tal como he comentado anteriormente la chiripa, impropiamente llamada en español serendipia, ha jugado un papel importante en el campo de la ciencia. Veamos dos ejemplos pegajosos de ella.
Los pegamentos siempre han sido unas sustancias usadas para diversos fines. En principio fueron de origen natural como la cola obtenida del colágeno de los peces cociendo las colas y las aletas -de ahí su nombre-, el engrudo elaborado con harina, la cera de abeja o el caucho natural, entre otros. Tiempo después se desarrollarían los pegamentos sintéticos, y aquí es donde comienza la historia de dos fracasos iniciales que acabaron dando resultados no previstos y a la larga sumamente exitosos.
En 1942 el químico norteamericano Harry Wesley Coover trabajaba para la empresa Eastman Kodak investigando polímeros con los que poder fabricar visores transparentes para ser utilizados en los visores de los fusiles; recordemos que Estados Unidos estaba entonces inmerso en la II Guerra Mundial. Estudiando uno de ellos se le adhirió a los prismas de un refractómetro con el que quería medir sus propiedades ópticas, resultando imposible limpiar el aparato al no poderse eliminar el tenaz polímero. Sin saberlo, y por supuesto sin pretender estropear irreversiblemente el delicado refractómetro, había descubierto al azar un pegamento de excepcionales propiedades adhesivas y solidificación instantánea, el cianocrilato, aunque en ese momento no valoró su potencial. Años después, ya terminada la guerra, Coover volvió a investigarlo apercibiéndose de su utilidad potencial, aunque no para los usos que había buscado sino como adhesivo. En 1958 se inició su fabricación y comercialización, convirtiéndose en uno de los pegamentos más utilizados actualmente. Aunque existen muchas marcas en el mercado, es conocido popularmente como loctite dado que fue esta compañía, tras cederle la patente Eastman Kodak, quien lo popularizó a partir de la década de 1960.
No menos curiosa es la historia de los post-it -otro nombre comercial, éste admitido por la RAE junto con la variante pósit-, esas etiquetas autoadhesivas que todos usamos para marcar páginas o dejar notas escritas, aunque paradójicamente se desarrolló en el sentido opuesto al anterior. En 1968 Spencer Ferguson Silver, también químico, trabajaba para la empresa 3M Company buscando un adhesivo extrafuerte que pudiera ser utilizado en la industria aeroespacial. Sin embargo uno de sus ensayos dio por resultado un compuesto que como pegamento era una auténtica birria, ya que su capacidad adhesiva era muy pequeña y se despegaba con facilidad, pero al mismo tiempo no perdía sus propiedades pudiéndose volver a pegar. Aunque Silver no fue capaz de prever la importancia de su accidental descubrimiento un colega suyo, Art Fry, fue el primero en aplicarlo en 1974 a un rectángulo de papel coloreado en forma de banda estrecha por uno de sus extremos; acababa de nacer el post-it. Su distribución comenzó en 1977 de forma limitada, y su comercialización a gran escala a partir de 1980 en los Estados Unidos y un año más tarde en Canadá y Europa. Se da la coincidencia de que el adhesivo de los post-it pertenece también a la familia de los acrilatos, aunque su estructura molecular es diferente de los cianoacrilatos.
Velocidades de vértigo

The Rocket (el Cohete), locomotora construida por Robert
Stephenson en 1829,
en el Museo de la Ciencia de Londres. Fotografía
tomada de la
Wikipedia
La invención del ferrocarril a principios del siglo XIX fue sin duda uno de los mayores avances tecnológicos de esta centuria, así como la extensión de la red ferroviaria por todos los continentes acarreó unos cambios sociales impensables hasta entonces, al tiempo que obligaba a acuerdos de índole mundial tales como la implantación del sistema de husos horarios en sustitución de los seculares horarios locales de cada población. En conjunto, se trató de unos cambios revolucionarios e irreversibles en la vida de muchos millones de personas, ya que por primera vez en la historia existía un medio de transporte rápido que en sus inicios alcanzaba unas velocidades medias de 30-40 kilómetros por hora; aunque ahora nos parezcan irrisorias, entonces era mucho más de lo que se podía alcanzar por medios tradicionales como los coches de caballos o las diligencias, y conforme se fue desarrollando la tecnología ferroviaria la diferencia fue haciéndose cada vez mayor.
Pese a las ventajas que acarreó el transporte ferroviario, tanto de pasajeros como de mercancías, éste se tuvo que enfrentar a críticas y protestas, en ocasiones razonables y en otras provocadas por intereses espurios de diversa índole: políticos, económicos, sociales, religiosos... que en determinadas ocasiones provocarían retrasos en el desarrollo de la red ferroviaria, desvíos de líneas e incluso supresión de su trazado. Éste es un tema extremadamente interesante, pero cae fuera del enfoque de esta sección.
Lo que sí voy a resaltar son algunas de las objeciones planteadas por los médicos de la época advirtiendo sobre los peligros que correrían los audaces pasajeros de los primeros trenes; y no, no era por riesgos presumibles tales como los accidentes y descarrilamientos o los atropellos, sino por cosas tan pintorescas como la presunción de que una velocidad mayor de 20 millas -unos 32 kilómetros- por hora provocaría la muerte por asfixia de los viajeros, algo que evidentemente no consta que ocurriera. También temían que las aceleraciones y las frenadas de los trenes causaran lesiones físicas, que la trepidación desatara enfermedades nerviosas, que el veloz paso del paisaje inflamara las retinas, que el polvo y el humo fomentaran las bronquitis, que el cambio excesivamente rápido -para la época- del clima de una ciudad al de otra afectara a las vías respiratorias, o que las embarazadas corrieran riesgo de abortar. Casi nada.
Si estos sesudos galenos resucitaran ahora y se les montara en un tren de alta velocidad, seguro que volverían despavoridos a sus tumbas.
Publicado el 12-12-2024
Actualizado el
30-1-2025
